TỔNG QUAN
Ung thư tụy là một trong những nguyên nhân hàng đầu gây tử vong do ung thư trên toàn thế giới, hiện đứng thứ tư về tỷ lệ tử vong ở cả nam và nữ. Bệnh thường ảnh hưởng đến những người lớn tuổi, với độ tuổi chẩn đoán trung bình là 71 tuổi đối với nam giới và 75 tuổi đối với nữ giới. Dữ liệu khu vực đông nam á cho thấy tỷ lệ mắc bệnh ước tính vào năm 2018 là khoảng 2,7 trường hợp ở nam giới và 1,7 trường hợp ở nữ giới trên 100.000 dân. Tỷ lệ này thấp hơn đáng kể so với các nước phương tây nhưng vẫn đòi hỏi sự chú trọng trong sàng lọc và phát hiện sớm.
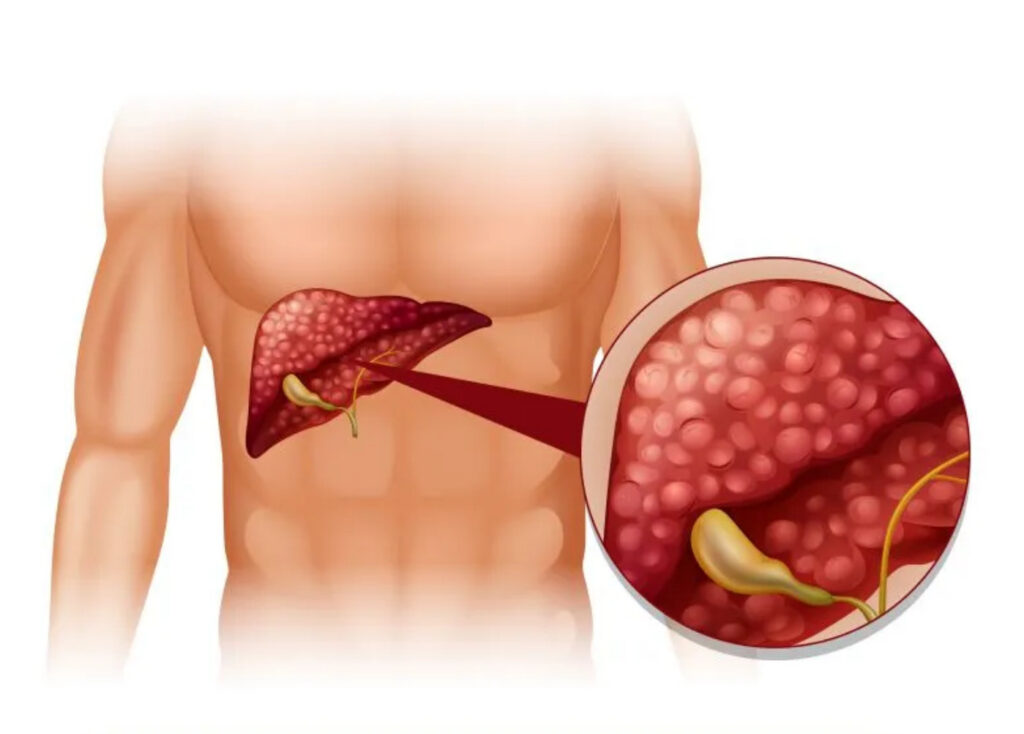
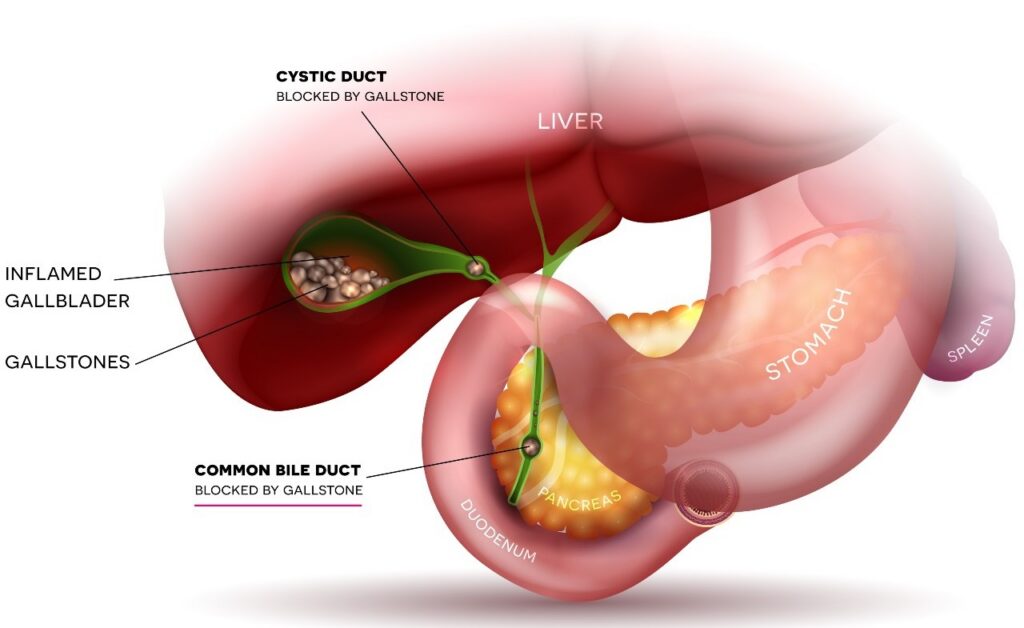
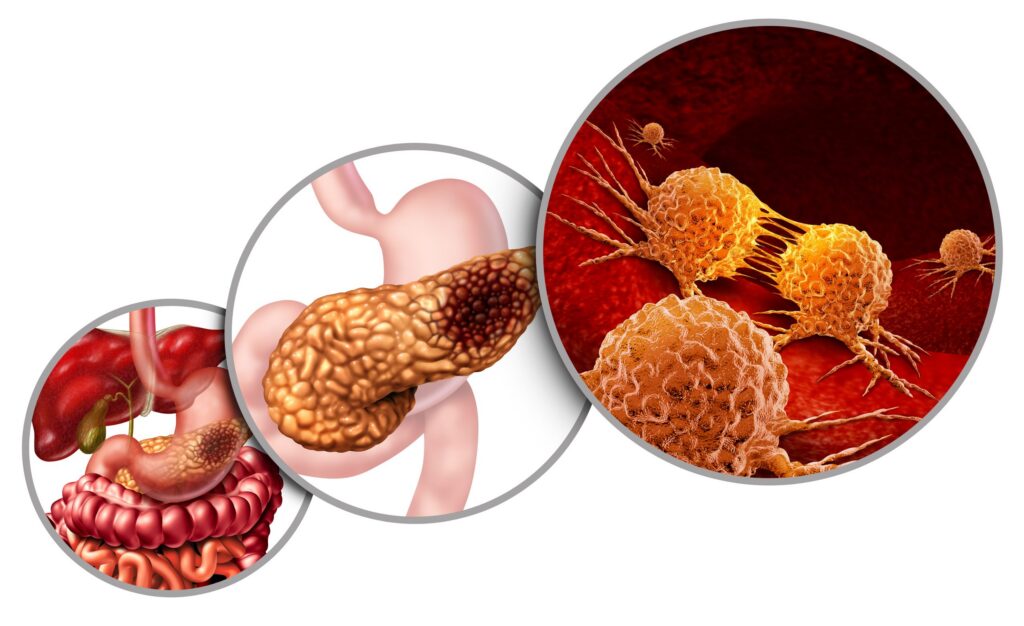
Tuyến tụy là một cơ quan có hình dạng giống chiếc lá, nằm sâu trong bụng, ngay phía sau dạ dày và được chia thành ba phần chính: đầu, thân và đuôi. Cơ quan này đóng vai trò quan trọng trong cơ thể với hai chức năng chính là nội tiết và ngoại tiết. Chức năng ngoại tiết được thực hiện bởi các tế bào sản xuất enzym tiêu hóa (như lipase, protease và amylase) giúp phân hủy chất béo, protein và carbohydrate trong ruột non. Trong khi đó, chức năng nội tiết được đảm nhiệm bởi các tế bào nằm trong “đảo tụy”, chịu trách nhiệm sản xuất các hormone quan trọng như insulin và glucagon trực tiếp vào máu để điều hòa đường huyết.
Ung thư tụy là tình trạng bệnh lý xảy ra khi các tế bào trong tuyến tụy bắt đầu phát triển và phân chia một cách không kiểm soát. Căn bệnh này thường được gọi là “kẻ giết người thầm lặng” vì ở giai đoạn đầu, các triệu chứng thường không rõ ràng hoặc dễ bị nhầm lẫn với các bệnh lý khác. Do tính chất xâm lấn mạnh mẽ, ung thư tụy thường chỉ được phát hiện khi đã ở giai đoạn tiến triển, gây khó khăn cho việc điều trị triệt để.
NGUYÊN NHÂN VÀ YẾU TỐ NGUY CƠ
- Nhóm yếu tố có thể thay đổi
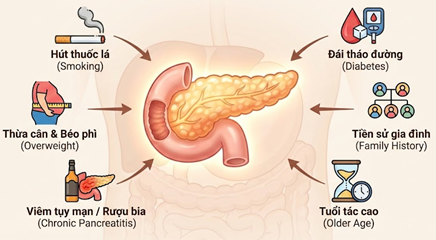
- Hút thuốc lá: Hút thuốc lá là một trong những yếu tố nguy cơ lớn nhất, chiếm khoảng 20-30% số ca ung thư tuyến tụy. Khói thuốc chứa hàng ngàn hóa chất độc hại có thể đi vào máu và gây tổn thương các tế bào tụy. Tin vui là, nguy cơ này sẽ giảm dần khi bạn quyết định bỏ thuốc.
- Thừa cân và béo phì: Những người có chỉ số khối cơ thể (BMI) cao có nguy cơ mắc bệnh cao hơn khoảng 20% so với người bình thường.
- Tiếp xúc với hóa chất độc hại: Làm việc lâu năm trong môi trường tiếp xúc nhiều với các hóa chất dùng trong ngành giặt khô, gia công kim loại hoặc thuốc trừ sâu.
- Nhóm yếu tố bệnh lý nền
- Đái tháo đường: Mối liên hệ giữa tiểu đường và ung thư tuyến tụy rất mật thiết. Nếu một người lớn tuổi (trên 50 tuổi) đột nhiên mắc tiểu đường dù cơ thể không béo phì hay không có tiền sử gia đình, thì đây có thể là một trong những dấu hiệu cảnh báo sớm hoặc là yếu tố nguy cơ cao của ung thư tụy.
- Viêm tụy mạn tính: Tình trạng viêm tụy kéo dài (thường do lạm dụng rượu bia hoặc hút thuốc lá) làm tổn thương các tế bào tụy liên tục, lâu ngày có thể dẫn đến ung thư tụy.
- Nhóm yếu tố không thể thay đổi
- Tuổi tác: Nguy cơ mắc bệnh tăng theo tuổi. Hầu hết bệnh nhân được chẩn đoán ở độ tuổi trên 65 tuổi.
- Tiền sử gia đình và đột biến gen: Nếu trong gia đình có cha mẹ, anh chị em ruột mắc bệnh, nguy cơ của bạn sẽ cao hơn. Y học hiện nay cũng nhấn mạnh vai trò của các đột biến gen di truyền, nổi bật nhất là đột biến gen BRCA1 và BRCA2
TRIỆU CHỨNG
Bạn cần ghi nhớ điều quan trọng nhất về ung thư tuyến tụy là ở giai đoạn đầu, bệnh thường “im hơi lặng tiếng” và rất ít khi gây ra triệu chứng rõ ràng. Các triệu chứng thường chỉ xuất hiện khi khối u đã đủ lớn để chèn ép vào các cơ quan lân cận hoặc xâm lấn vào các dây thần kinh.
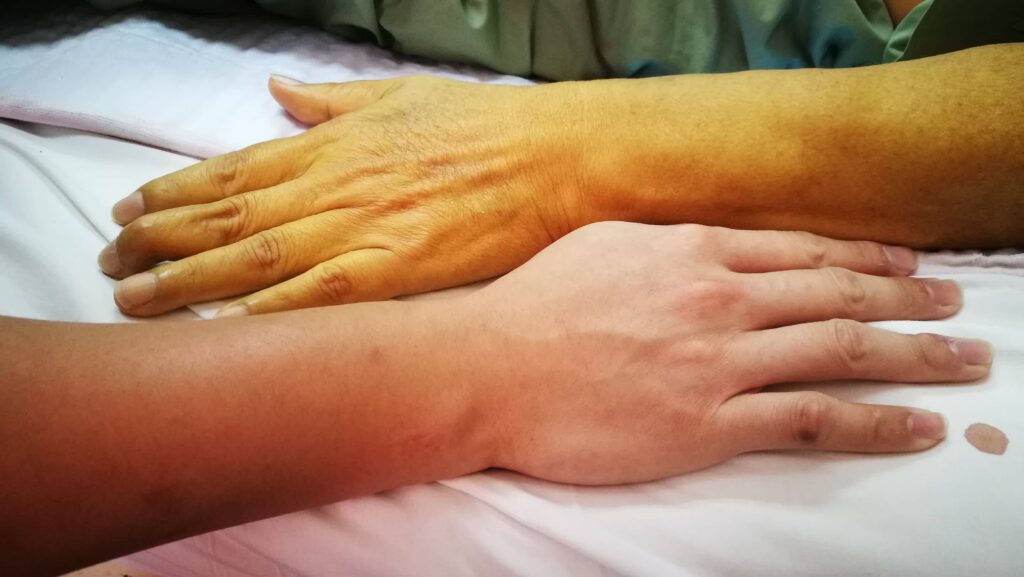
- Vàng da và vàng mắt kèm ngứa
- Thay đổi màu sắc nước tiểu và phân:
- Nước tiểu sẫm màu
- Phân bạc màu (Màu đất sét)
- Đau bụng: Cơn đau thường âm ỉ, mơ hồ ở vùng thượng vị (vùng bụng trên rốn).
- Sụt cân không rõ nguyên nhân, chán ăn: Cơ thể đột ngột sụt cân nhanh chóng dù bạn không hề ăn kiêng hay tập luyện gắng sức. Kèm theo đó là cảm giác chán ăn, cơ thể suy nhược.
- Các vấn đề tiêu hóa khác: Buồn nôn, nôn mửa, cảm giác đầy bụng, khó tiêu hoặc cảm thấy no rất nhanh sau khi ăn một lượng nhỏ thức ăn (do khối u chèn ép vào dạ dày)
CHẨN ĐOÁN
- Xét nghiệm
- CA 19-9 là dấu ấn sinh học phổ biến nhất trong ung thư tụy. Chỉ số này tăng giúp phân biệt giữa ung thư và các tổn thương lành tính, đồng thời là cơ sở để theo dõi đáp ứng với điều trị và theo dõi tái phát sau phẫu thuật. Tuy nhiên, CA 19-9 có thể tăng trong các trường hợp lành tính như tắc mật hoặc viêm tụy.
- Các xét nghiệm máu khác: Xét nghiệm chức năng gan, xét nghiệm Bilirubin trong máu để đánh giá tình trạng tắc mật, cùng với xét nghiệm công thức máu toàn bộ và đường huyết để phát hiện đái tháo đường.
- Sinh thiết lỏng: Các nghiên cứu hiện đại đang phát triển kỹ thuật sinh thiết lỏng dựa trên exosome (các túi nhỏ do tế bào tiết ra) và bảng xét nghiệm bốn dấu ấn sinh học (CA 19-9, THBS2, ANPEP, PIGR). Những phương pháp này cho thấy độ chính xác lên tới hơn 90% trong việc phát hiện bệnh ở giai đoạn sớm (giai đoạn I và II), mở ra hy vọng cải thiện tiên lượng sống cho bệnh nhân.
- Các phương tiện chẩn đoán hình ảnh học
- Chụp cắt lớp vi tính (CT Scan): giúp đánh giá chi tiết sự xâm lấn của khối u vào các động mạch và tĩnh mạch lân cận, từ đó quyết định khối u còn khả năng cắt bỏ hay không.
- Chụp cộng hưởng từ (MRI) thường được chỉ định ở các trường hợp mà hình ảnh không rõ ràng trên phim CT. MRI đặc biệt ưu thế trong việc phát hiện các tổn thương di căn nhỏ ở gan mà CT có thể bỏ sót.
- Siêu âm nội soi (EUS): Đây là kỹ thuật giúp phát hiện các khối u có kích thước nhỏ (< 2 cm). Bằng cách đưa đầu dò siêu âm vào sát dạ dày và tá tràng, bác sĩ có thể quan sát tụy một cách trực tiếp mà không bị cản trở bởi hơi trong ruột.
- Sinh thiết
- Kỹ thuật EUS-FNA (Chọc hút kim nhỏ dưới hướng dẫn của siêu âm nội soi): Đây là kỹ thuật ưu tiên hàng đầu để thu thập mẫu mô từ tụy.
- Mục đích của sinh thiết: Ngoài việc xác nhận sự hiện diện của tế bào ung thư, sinh thiết còn giúp bác sĩ phân biệt giữa ung thư biểu mô tuyến (Adenocarcinoma – chiếm khoảng 95%) với các loại u ít gặp hơn như u nội tiết tụy (PNET) vốn có cách điều trị hoàn toàn khác.
- Xét nghiệm di truyền: Mẫu mô lấy được có thể dùng để kiểm tra các đột biến gen quan trọng như BRCA1, BRCA2 hay PALB2. Việc này không chỉ giúp gia đình bệnh nhân có kế hoạch tầm soát phù hợp mà còn giúp bác sĩ lựa chọn các loại thuốc điều trị đích mới (như thuốc ức chế PARP) mang lại hiệu quả cao hơn.
CÁC PHƯƠNG PHÁP ĐIỀU TRỊ
Phẫu thuật là phương pháp cắt bỏ khối u tụy. Tuy nhiên, thực tế chỉ có khoảng 15-20% bệnh nhân đủ điều kiện phẫu thuật tại thời điểm chẩn đoán vì khối u thường đã lan rộng hoặc xâm lấn mạch máu. Các phương pháp phẫu thuật hiện nay bao gồm:
- Phẫu thuật cắt khối tá tụy: Phẫu thuật này dành cho khối u ở đầu tụy. Đầu tụy, tá tràng, túi mật, một phần ống mật chủ và đôi khi là một phần dạ dày được cắt bỏ. Sau đó, các cơ quan còn lại sẽ được nối với ruột non để tái lập lưu thông tiêu hóa.
- Cắt tụy đoạn thân và đuôi: Dành cho khối u nằm ở phần giữa hoặc phần cuối của tuyến tụy, thường kèm theo cắt lách
- Cắt toàn bộ tuyến tụy: Bác sĩ sẽ cắt bỏ toàn bộ tụy nếu khối u lan rộng. Sau phẫu thuật này, bệnh nhân sẽ phải sử dụng insulin và enzyme tụy suốt đời để điều hòa đường huyết và chức năng tiêu hóa.
Hóa trị là phương pháp sử dụng thuốc để tiêu diệt tế bào ung thư hoặc ngăn chúng phân chia. Phương pháp này có thể được dùng độc lập hoặc phối hợp với các phương pháp khác.
- Hóa trị trước phẫu thuật: Làm nhỏ khối u nhằm làm cho khối u có khả năng cắt bỏ được.
- Hóa trị sau phẫu thuật: Để tiêu diệt những tế bào ung thư còn sót lại và giảm nguy cơ tái phát.
- Các phác đồ phổ biến: FOLFIRINOX (phối hợp 4 loại thuốc) thường mang lại hiệu quả cao nhưng có thể gây nhiều tác dụng phụ, hoặc Gemcitabine kết hợp Nab-paclitaxel
Xạ trị dùng các tia năng lượng cao để phá hủy tế bào ung thư
- Hóa-xạ trị đồng thời: Thường được dùng để kiểm soát khối u tại chỗ, đặc biệt là ở giai đoạn tiến triển tại chỗ không thể phẫu thuật.
- Xạ trị định vị thân (SBRT): Là kỹ thuật sử dụng liều bức xạ cao, chính xác vào khối u trong thời gian ngắn (thường từ 1-5 ngày), giúp hạn chế tổn thương mô lành xung quanh.
Các liệu pháp tiến bộ và mới nhất hiện nay:
- Liệu pháp trúng đích (Thuốc ức chế PARP): Những thuốc như Olaparib dành riêng cho bệnh nhân có đột biến gen BRCA1 hoặc BRCA2.
- Thiết bị điện trường (TTFields): Thiết bị đeo mang tên Optune Pax vừa được FDA chấp thuận năm 2026. Thiết bị này phát ra điện trường để ức chế sự phân chia tế bào ung thư mà không ảnh hưởng nhiều đến tế bào khỏe mạnh.
- Liệu pháp miễn dịch: Các thuốc như Pembrolizumab đang được nghiên cứu để kích thích hệ miễn dịch của chính cơ thể tấn công khối u.
Chăm sóc hỗ trợ và giảm nhẹ mục tiêu là giúp bệnh nhân có chất lượng cuộc sống tốt hơn nhờ vào việc điều trị các triệu chứng, tác dụng phụ.
- Kiểm soát đau: Dùng thuốc giảm đau mạnh hoặc thực hiện thủ thuật phong bế đám rối tạng.
- Hỗ trợ tiêu hóa: Bổ sung enzyme tụy dạng viên uống giúp giải quyết tình trạng phân mỡ, tiêu chảy.
- Giải quyết tình trạng tắc mật: Nếu khối u chèn ép ống mật gây vàng da, bác sĩ sẽ đặt một ống thông nhỏ (stent) để giải thông đường mật.
KHI NÀO CẦN GẶP BÁC SĨ?
Ung thư tuỵ là một bệnh lý nguy hiểm nhưng diễn tiến hết sức thầm lặng. Tầm soát được dành riêng cho những cá nhân có nguy cơ cao do di truyền hoặc tiền sử gia đình, bao gồm:
- Những người mang đột biến gen liên quan đến ung thư như BRCA1, BRCA2, PALB2, ATM.
- Người mắc các hội chứng di truyền như hội chứng Peutz-Jeghers, hội chứng Lynch, hoặc viêm tụy di truyền.
- Gia đình có từ hai người thân trực hệ (cha mẹ, anh chị em, con cái) trở lên mắc ung thư tụy.
Các phương pháp tầm soát chính gồm chụp cộng hưởng từ, siêu âm nội soi
Thời điểm tầm soát tùy thuộc vào loại đột biến gen hoặc độ tuổi của người thân trẻ nhất trong gia đình mắc bệnh (thường bắt đầu từ tuổi 50, nhưng có thể sớm hơn như tuổi 35 đối với hội chứng Peutz-Jeghers).